Standardaminosäuren
Eine der nützlichsten Methoden zur Klassifizierung der Standardaminosäuren (oder der üblichen Aminosäuren) basiert auf der Polarität (dh der Verteilung der elektrischen Ladung) der R-Gruppe (z. B. Seitenkette).
Gruppe I: Unpolare Aminosäuren
Aminosäuren der Gruppe I sind Glycin, Alanin, Valin, Leucin, Isoleucin, Prolin, Phenylalanin, Methionin und Tryptophan. Die R-Gruppen dieser Aminosäuren haben entweder aliphatische oder aromatische Gruppen. Dies macht sie hydrophob ("wasserangst"). In wässrigen Lösungen falten sich globuläre Proteine in eine dreidimensionale Form, um diese hydrophoben Seitenketten im Proteininneren zu vergraben. Die chemischen Strukturen von Aminosäuren der Gruppe I sind:
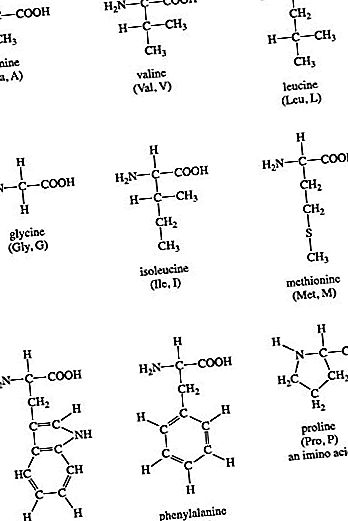
Isoleucin ist ein Isomer von Leucin und enthält zwei chirale Kohlenstoffatome. Prolin ist unter den Standardaminosäuren insofern einzigartig, als es nicht sowohl freie α-Amino- als auch freie α-Carboxylgruppen aufweist. Stattdessen bildet seine Seitenkette eine cyclische Struktur, da das Stickstoffatom von Prolin an zwei Kohlenstoffatome gebunden ist. (Streng genommen bedeutet dies, dass Prolin keine Aminosäure, sondern eine α-Iminosäure ist.) Phenylalanin besteht, wie der Name schon sagt, aus einer an Alanin gebundenen Phenylgruppe. Methionin ist eine der beiden Aminosäuren, die ein Schwefelatom besitzen. Methionin spielt eine zentrale Rolle bei der Proteinbiosynthese (Translation), da es fast immer die initiierende Aminosäure ist. Methionin liefert auch Methylgruppen für den Stoffwechsel. Tryptophan enthält einen Indolring, der an die Alanylseitenkette gebunden ist.
Gruppe II: Polare, ungeladene Aminosäuren
Aminosäuren der Gruppe II sind Serin, Cystein, Threonin, Tyrosin, Asparagin und Glutamin. Die Seitenketten in dieser Gruppe besitzen ein Spektrum an funktionellen Gruppen. Die meisten haben jedoch mindestens ein Atom (Stickstoff, Sauerstoff oder Schwefel) mit Elektronenpaaren zur Wasserstoffbindung an Wasser und andere Moleküle. Die chemischen Strukturen von Aminosäuren der Gruppe II sind:

Zwei Aminosäuren, Serin und Threonin, enthalten aliphatische Hydroxylgruppen (dh ein Sauerstoffatom, das an ein Wasserstoffatom gebunden ist und als ―OH dargestellt wird). Tyrosin besitzt eine Hydroxylgruppe im aromatischen Ring, was es zu einem Phenolderivat macht. Die Hydroxylgruppen in diesen drei Aminosäuren unterliegen einer wichtigen Art der posttranslationalen Modifikation: der Phosphorylierung (siehe unten Nichtstandardisierte Aminosäuren). Cystein enthält wie Methionin ein Schwefelatom. Im Gegensatz zum Schwefelatom von Methionin ist der Schwefel von Cystein jedoch chemisch sehr reaktiv (siehe unten Cysteinoxidation). Asparagin, das zuerst aus Spargel isoliert wurde, und Glutamin enthalten beide Amid-R-Gruppen. Die Carbonylgruppe kann als Wasserstoffbindungsakzeptor fungieren, und die Aminogruppe (NH 2) kann als Wasserstoffbindungsdonor fungieren.
Gruppe III: Saure Aminosäuren
Die zwei Aminosäuren in dieser Gruppe sind Asparaginsäure und Glutaminsäure. Jedes hat eine Carbonsäure an seiner Seitenkette, die ihm saure (protonenspendende) Eigenschaften verleiht. In einer wässrigen Lösung bei physiologischem pH-Wert ionisieren alle drei funktionellen Gruppen dieser Aminosäuren und ergeben eine Gesamtladung von -1. In den ionischen Formen werden die Aminosäuren Aspartat und Glutamat genannt. Die chemischen Strukturen von Aminosäuren der Gruppe III sind

Die Seitenketten von Aspartat und Glutamat können Ionenbindungen („Salzbrücken“) bilden und auch als Wasserstoffbrückenakzeptoren fungieren. Viele Proteine, die Metallionen ("Metalloproteine") für strukturelle oder funktionelle Zwecke binden, besitzen Metallbindungsstellen, die Aspartat- oder Glutamat-Seitenketten oder beides enthalten. Freies Glutamat und Glutamin spielen eine zentrale Rolle im Aminosäurestoffwechsel. Glutamat ist der am häufigsten vorkommende exzitatorische Neurotransmitter im Zentralnervensystem.








![Der gute, der schlechte und der hässliche Film von Leone [1966] Der gute, der schlechte und der hässliche Film von Leone [1966]](https://images.thetopknowledge.com/img/entertainment-pop-culture/2/good-bad-ugly-film-leone-1966.jpg)




