Gesetz bestimmter Proportionen, Aussage, dass jede chemische Verbindung feste und konstante Anteile (nach Masse) ihrer Bestandteile enthält. Obwohl viele Experimentatoren lange Zeit die Wahrheit des Prinzips im Allgemeinen angenommen hatten, sammelte der französische Chemiker Joseph-Louis Proust in einer Reihe von Untersuchungen zur Zusammensetzung vieler Substanzen, insbesondere der Eisenoxide, erstmals schlüssige Beweise dafür (1797). Ein anderer französischer Chemiker, Claude Berthollet, der für unbestimmte Anteile hielt, bestritt Prousts Ergebnisse, aber der schottische Chemiker Thomas Thomson bestätigte einige davon und schrieb in seinem Artikel „Chemie“ in der Beilage zur Enzyklopädie (1801), dass Proust definitiv bewiesen habe, „ Metalle sind nicht zu unbestimmten Oxidationsgraden fähig. “ Das Prinzip wurde dann vom englischen Chemiker John Dalton in seiner chemischen Atomtheorie (1808) konkret formuliert.
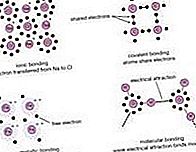
chemische Bindung: Das Gesetz bestimmter Proportionen
Lavoisiers Experimente inspirierten weitere Studien, die letztendlich zu einem Sturz der Ansicht führten, dass Materie strukturlos ist









![Der Lohn der Angst Film von Clouzot [1953] Der Lohn der Angst Film von Clouzot [1953]](https://images.thetopknowledge.com/img/entertainment-pop-culture/4/wages-fear-film-clouzot-1953.jpg)



