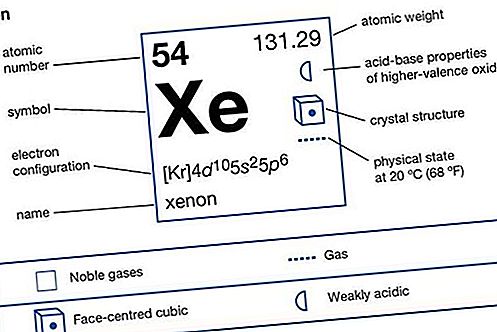
Xenon (Xe), chemisches Element, ein schweres und äußerst seltenes Gas der Gruppe 18 (Edelgase) des Periodensystems. Es war das erste Edelgas, das echte chemische Verbindungen bildete. Xenon ist mehr als 4,5-mal schwerer als Luft und farblos, geruchlos und geschmacklos. Festes Xenon gehört zum flächenzentrierten kubischen Kristallsystem, was bedeutet, dass sich seine Moleküle, die aus einzelnen Atomen bestehen, wie Kugeln verhalten, die so eng wie möglich zusammengepackt sind. Der Name Xenon leitet sich vom griechischen Wort Xenos ab, "seltsam" oder "fremd".

Edelgas
(Ar), Krypton (Kr), Xenon (Xe), Radon (Rn) und Oganesson (Og). Die Edelgase sind farblose, geruchlose, geschmacksneutrale, nicht brennbare Gase.
.Elementeigenschaften
| Ordnungszahl | 54 |
|---|---|
| atomares Gewicht | 131,29 |
| Schmelzpunkt | –111,9 ° C (–169,4 ° F) |
| Siedepunkt | –108,0 ° C (–162,4 ° F) |
| Dichte (1 atm, 0 ° C) | 5,887 g / Liter (0,078 Unzen / Gallone) |
| Oxidationsstufen | 0, +2, +4, +6, +8 |
| Elektronenkonfiguration | (Kr) 4d 10 5s 2 5p 6 |
Eigenschaften des Elements
Xenon kommt in leichten Spuren in Gasen innerhalb der Erde vor und ist in einem Ausmaß von etwa 0,0000086 Prozent oder etwa 1 Teil von 10 Millionen Volumen trockener Luft vorhanden. Wie mehrere andere Edelgase ist Xenon in Meteoriten vorhanden. Xenon wird im kleinen Maßstab durch fraktionierte Destillation von flüssiger Luft hergestellt. Es ist das am wenigsten flüchtige (Siedepunkt –108,0 ° C [–162,4 ° F]) der aus der Luft erhältlichen Edelgase. Die britischen Chemiker Sir William Ramsay und Morris W. Travers isolierten das Element 1898 durch wiederholte fraktionierte Destillation des Edelgas-Kryptons, das sie sechs Wochen zuvor entdeckt hatten.
Das Element Xenon wird in Lampen verwendet, die extrem kurze und intensive Lichtblitze erzeugen, wie Stroboskope und Lichter für die Hochgeschwindigkeitsfotografie. Wenn eine Ladung Elektrizität mit niedrigem Druck durch das Gas geleitet wird, sendet sie einen bläulich-weißen Lichtblitz aus. Bei höheren Drücken wird weißes Licht emittiert, das dem Tageslicht ähnelt. Xenon-Taschenlampen werden verwendet, um Rubinlaser zu aktivieren.
Natürliches Xenon ist eine Mischung aus neun stabilen Isotopen in den folgenden Prozentsätzen: Xenon-124 (0,096), Xenon-126 (0,090), Xenon-128 (1,92), Xenon-129 (26,44), Xenon-130 (4,08), Xenon -131 (21,18), Xenon-132 (26,89), Xenon-134 (10,44) und Xenon-136 (8,87). Die Massenzahlen der bekannten Xenonisotope liegen zwischen 118 und 144. Das in einigen steinigen Meteoriten gefundene Xenon zeigt einen großen Anteil an Xenon-129, von dem angenommen wird, dass es ein Produkt des radioaktiven Zerfalls von Jod-129 ist, dessen Halbwertszeit 17.000.000 beträgt Jahre. Die Messung des Xenon-129-Gehalts von Meteoriten wirft ein Licht auf die Geschichte des Sonnensystems. Mehr als ein Dutzend radioaktiver Xenonisotope, die durch Spaltung von Uran und andere Kernreaktionen hergestellt werden, sind bekannt. Beispielsweise wird Xenon-135 (Halbwertszeit 9,2 Stunden) durch Uranspaltung in Kernreaktoren hergestellt, wo es problematisch ist, weil es spaltproduzierende Neutronen absorbiert. Xenon-129 ist von besonderer Bedeutung, da dieses Isotop durch Kernspinresonanzspektroskopie beobachtet werden kann, was es für die strukturelle Charakterisierung von Xenonverbindungen nützlich macht. Die Xenon-Isotope, die in der größten Menge durch Kernspaltung erzeugt werden, sind Xenon-131, -132, -134 und -136, die stabil sind, und Xenon-133, das radioaktiv ist, mit einer Halbwertszeit von 5,27 Tagen.













